バッテリーの仕組みと劣化
バッテリーの内部
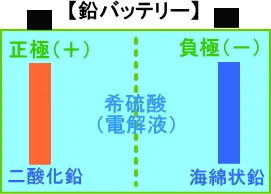
バッテリーの基本的な内部構造は、正極板に二酸化鉛(PbO2)、負極板に海綿状鉛(Pb)が使用され、これらが電解液としての希硫酸(H2SO4)に満たされた状態となっています。
放電
自動車やバイクのエンジンがかかっておらずオルタネーターからの充電が行われていない状態で、室内灯を点灯させたり、オーディオなどのアクセサリー類を使用したりする場合は、バッテリーがその電力を供給することとなります。
この時、正極板、負極板それぞれは下記の様な反応が行われ電子(電流)が発生します。
正極板
正極板(PbO2)が、負極板の化学反応で発生した電子(2e-)を受け取り、硫酸鉛(PbSO4)と水(H2O)に変化します。
負極板
海綿状鉛(Pb)が硫酸鉛(PbSO4)に変化し、電子(2e-)を発生します。
この結果、放電が進むと、希硫酸より比重の軽い水(H2O)の割合が増える為、バッテリー液(電解液)の比重を測定することで、バッテリーの消耗度合を測定することが出来ます。
放電時のバッテリー全体の反応式
PbSO4+2H2SO4+Pb=>PbSO4+2H2O+PbSO4
充電
自動車やバイクが走行するとオルタネーターによりバッテリーに充電が行われます。
この時、正極板、負極板それぞれは下記の様な反応が行われ正極板、負極板とも、もとの二酸化鉛と海綿状鉛に戻ります。
正極板
水が電気分解され、正極板は硫酸鉛(PbSO4)から二酸化鉛(PbO2)に戻り、電解液も希硫酸(H2SO4)に戻ります。
負極板
充電されることにより、電子(2e-)を受け取り、もとの海綿状鉛(Pb)と電解液も希硫酸(H2SO4)に戻ります。
充電時のバッテリー全体の反応式は、
PbSO4+2H2O+PbSO4==>PbO2+2H2SO4+Pb
となります。
バッテリーの劣化
上記の化学式では、放電<=>充電が完全に等しく行われていますが、実際は、バッテリーが充放電を繰り返すうちに、放電時に硫酸鉛(PbSO4)変化した結晶化し(サルフレーション)、電気が流れにくくなり劣化します。
バッテリー上がりに24時間対応
突然発生するバッテリー上がりに深夜 早朝24時間受付のコールセンターが安心の対応を致します。
お困りの際は、お気軽にお問い合わせください。
生活当番24受付センター
電話 050-2018-0667
お客様に最短時間で対応できる作業員を緊急手配致します。
